
高血压人群在选用降压药的时候,经常会面临这样的现象:
使用A药物,血压控制不佳;换用B药物后,降压效果可能不错但又出现明显的不良反应;换用C药物后,不良反应消除了,但血压仍未得到有效的控制住;换用降压药D之后,患者的血压才得以控制!这个漫长的“试药”路,不仅给高血压人群健康带来了很大风险,而且也带来一定的经济负担。
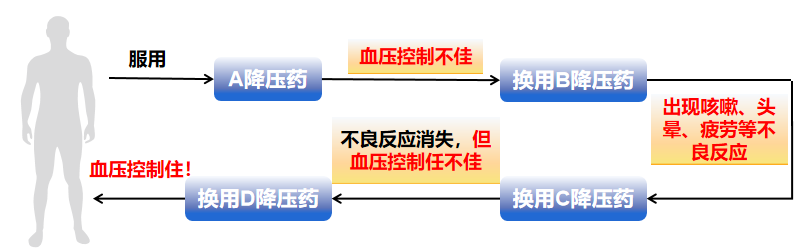
基因检测,这一“量体裁衣”的个体化用药指导方案,可通过一次检测,为每一位高血压患者筛选出疗效最佳,不良反应及毒副作用最小的降压药。
不管是单药治疗,还是联合治疗,每一步都有几种不同方案。怎么选?逐个尝试?有没有更好的办法?基因组学的研究给我们带来了新的解决办法!
2017年指南建议基因检测指导降压药物应用
高血压合理用药指南(第 2 版) 指出:药物基因组学已成为指导临床个体化用药、评估严重药物不良反应发生风险的重要工具。通过检测药物代谢酶和药物靶点基因,可指导临床医生针对特定患者选择合适的降压药物和给药剂量,提高降压药物治疗的有效性和安全性。
ARB与基因多态性
不同个体对于药物反应的差异性很大,影响因素包括年龄、并发症、营养状况、遗传因素、药物相互作用及环境等,其中遗传因素的影响尤为重要。药物进入人体内,经过吸收、转运、代谢、效应及清除的过程发挥作用,携带不同基因型的患者在上述药物作用过程中可能呈现反应的程度不同,表现为药物反应性的个体差异。
ARB的抗高血压反应因患者而异,并且涉及药物靶向受体和药物代谢的基因中的单核苷酸多态性 (SNP) 与这种个体差异有关 。
血管紧张素Ⅱ受体拮抗剂(ARB)是继血管紧张素转换酶抑制剂(ACEI)之后又一类作用于RAS的重要药物,通过阻断血管紧张素Ⅱ与受体结合,调节血管紧张素Ⅱ的大多数心血管效应。它作用于RAS的末端受体水平,更充分、更直接、更具选择性地阻断RAS,且不具有干咳、血管神经水肿等不良反应。
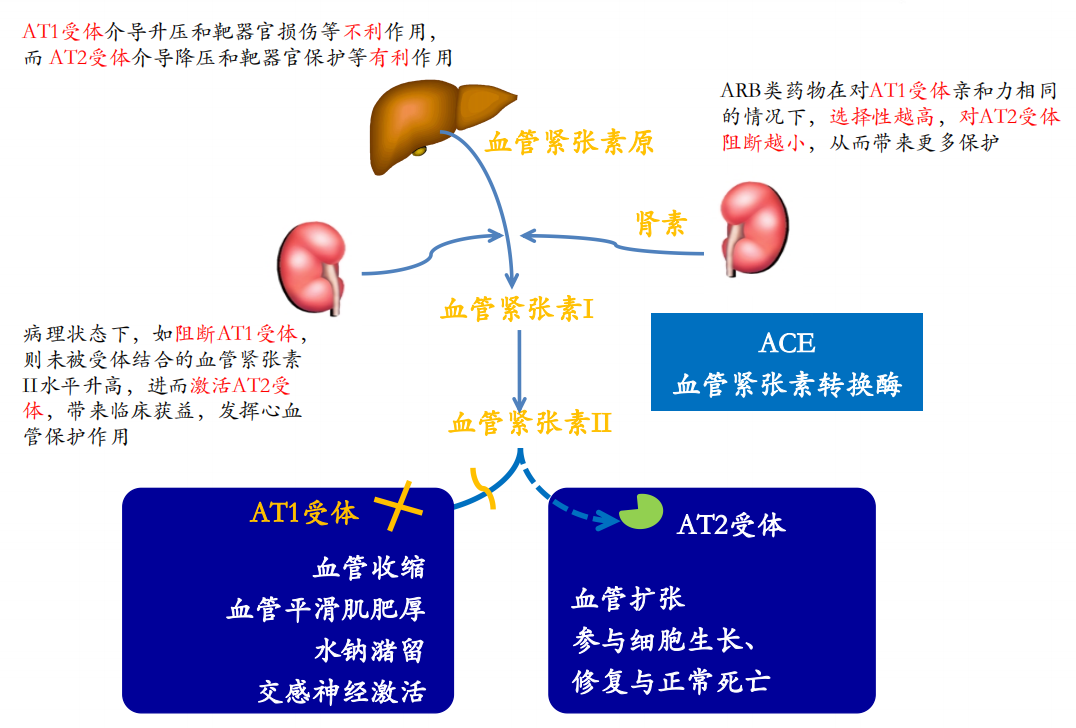
药物发挥作用的各个环节都可能因基因变异而表现出明显的差异性反应。多项研究表明,AGTR1和CYP2C9基因中的SNP有助于ARB的抗高血压作用。
氯沙坦与CYP2C9
ARBs主要由CYP2C9基因编码的肝细胞色素P450 2C9 (CYP2C9) 代谢并转化为非活性/活性形式 。
氯沙坦需通过CYP2C9将氯沙坦代谢为E-3174(其活性是氯沙坦的40倍)。CYP2C9*3基因多态性会导致酶活性降低,携带*3等位基因的个体比具有CYP2C9*1/*1(野生型)的个体代谢差,影响氯沙坦的治疗效果。
据研究报道在健康人群中每人口服50mg氯沙坦片,检测24h内的血药浓度变化,结果发现携带CYP2C9*1/*3和*3/*3基因型的患者氯沙坦药时曲线下面积与其代谢活性产物之比分别比野生型高出2倍和30倍。
厄贝沙坦与CYP2C9
与氯沙坦不同,厄贝沙坦需要CYP2C9 转化为无活性代谢物。CYP2C9*3/*3基因突变型服用厄贝沙坦清除速率降低,血药浓度增加,不良反应风险可能会增加。
一项研究数据显示,口服150mg厄贝沙坦后36h内受试者的血药浓度变化。结果发现CYP2C9*1/*3的最高血药浓度分别比CYP2C9*1/*1高1.56倍和1.5倍,半衰期高1.38倍和1.5倍,同时体清除率比CYP2C9*1/*1低39.3%和44.0%。
缬沙坦与AGTR1
ARB通过阻断由AGTR1基因编码的血管紧张素 II 受体 type1 (AGTR1) 表现出降低血压的作用,AGTR1基因的多态性导致个体对药物产生了差异性。
中日友好医院的一项纳入281名患者的回顾性研究中发现,服用缬沙坦控制良好的患者中检测到的C等位基因和AC+CC基因型的频率高于控制不佳的患者,与AA基因型相比,AGTR1 A1166C的CC+AC基因型与缬沙坦治疗更好地控制高血压显着相关。